这是什么病毒?!《Science》长文:“它与人类所见过的任何病原体都不一样”
摘自《国际科学》
随着全球确诊的COVID-19病例数量激增,目前感染人数已超过240万,死亡人数超过16万人,临床医生和病理学家正在努力了解冠状病毒对人体造成的损害。
他们意识到,虽然肺部是受感染最严重的器官,但它可以延伸到包括心脏和血管、肾脏、肠道和大脑在内的许多其他器官。

图片转自Pixabay
耶鲁大学和耶鲁-纽黑文医院的心脏病学家Harlan Krumholz说:“这种疾病几乎可以攻击人体内的任何一样组织器官,这种持续性攻击的结果将是毁灭性的。”
2020年4月17日,《Science》发表最新文章,为大家详细介绍了新型冠状病毒对于人体多个脏器的攻击。文章题目为《How does coronavirus kill? Clinicians trace a ferocious rampage through the body, from brain to toes》,中文译名为《冠状病毒是如何杀死人的?临床医生们追踪其对于人体从头到脚的攻击》。

理解这一病毒的强进攻性可以帮助一线医生治疗那些其他部位病变的陷入绝望的感染者。
比如,新近观察到的凝血倾向是否会将一些轻症病例转变为重症病例?在最坏的情况下,是否有过度的免疫反应?使用免疫抑制药物进行治疗是否会有帮助?如何解释一些医生报告的患者血氧水平低得惊人,但他们却没有呼吸困难?
以下是关于病毒如何快速攻击人体细胞的认识,这些数据主要来自危重病人身上。尽管现在每周都有1000多篇论文对SARS-CoV-2病毒及COVID-19进行探讨,但由于这种病毒的行为方式与人类所见过的任何病原体都不一样,所以很难对它有一个清晰的认识。
如果没有更大规模的前瞻性对照研究,科学家们就必须从小型研究和案例报告中获取信息。然而小型研究往往样本量较小且都是通过快速审查发表,因此可能并没有同行评议。
拉什大学医学中心(Rush University Medical Center)的肝脏移植医生Nancy Reau说道:“面对这一情况,我们只能保持一种非常开放的心态,我们在通过不同的病例报道不断学习。”
体内感染的开始
当感染者排出携带病毒的飞沫被其他人吸入后,新型冠状病毒(SARS-CoV-2)就会进入吸入者的鼻腔和咽喉。它在新的鼻腔内找到了新的家。
鼻腔里的细胞富含一种叫做血管紧张素转换酶2 (ACE2)的细胞表面受体。在人体各处,ACE2通常有助于血压的调节,但是它的存在也意味着感染的开始。
病毒通过这种受体真正的进入细胞。一旦进入细胞内部,病毒就会利用细胞内的细胞器,制造无数个病毒拷贝。
随着病毒的繁殖,在第一周左右,感染者体内会产生大量的病毒。此时感染者可能并不存在任何症状,但也可能会出现发烧、干咳、喉咙痛、嗅觉和味觉丧失,或者头痛和身体疼痛等不适症状。
图片转自Pixabay
如果免疫系统在最初阶段没有击退SARS-CoV-2,那么病毒就会沿着气管向下蔓延,攻击肺部,在肺部才真正发展为致命性的病毒。肺部支气管的末端膨大为肺,每个肺泡由单层细胞排列,这些细胞富含ACE2受体。
正常情况下,氧气通过肺泡进入毛细血管(毛细血管是位于肺泡旁的微小血管),然后氧气通过血液被输送到身体的其他部位。但是当免疫系统与入侵者作战时,战斗本身就会破坏这种健康的氧气传输过程。
前线的白细胞释放一种叫做趋化因子的炎症分子,这些趋化因子反过来又会召唤更多的免疫细胞来瞄准并杀死被病毒感染的细胞,留下大量的液体和死细胞。
这是肺炎的基本病理过程,伴有相应的症状,包括咳嗽、发烧、呼吸浅快,这在COVID-19患者中非常常见。
但是病情可能突然恶化,发展成一种叫做急性呼吸窘迫综合症(ARDS)的疾病。这时,患者血液中的氧气含量急剧下降,呼吸变得更加困难。
在X光和计算机断层扫描中,他们的肺部被白色的混浊物打得千疮百孔。一般情况下,这些病人最终需要使用呼吸机。
许多尸体解剖显示,他们的肺泡里充满了液体、白细胞、粘液和被破坏的肺细胞的碎屑,这实际就是免疫细胞与病毒对战后的真实战场。
病毒的深入影响——细胞因子风暴
虽然SARS-CoV-2会进入肺部,对肺部造成严重损害,但是实际上病毒影响范围不仅局限于肺部。科学家们才刚刚开始探索这种危害的范围和性质。
一些临床医生怀疑,许多重症患者情况越来越差可能是免疫系统的过度反应导致的,即所谓的“细胞因子风暴”,实际上许多病毒感染都会引发这种反应,比如埃博拉病毒。
细胞因子是化学信号分子,正常情况下它介导着一个健康的免疫反应,帮助抵御外来病毒的入侵,但在细胞因子风暴中,某些细胞因子的水平飙升,远远超过所需水平,免疫细胞开始无差别攻击健康组织,最终导致血管泄漏、血压下降、血栓形成、器官衰竭和死亡。换句话说,这几乎等同于免疫系统启动的“自毁程序”,选择和病毒同归于尽。
一些研究表明,住院的COVID-19患者血液中这些炎症诱导细胞因子水平升高。坦普尔大学医院(Temple University Hospital)肺病学家Jamie Garfield认为:“这种疾病的实际发病率和死亡率可能是由对机体应对病毒时产生的过度炎症反应造成的。”
但并不是所有人都认同这一观点,斯坦福大学医学院(Stanford University School or Medicine)肺部危重症护理医师Joseph Levitt表示:“虽然人们很快就将COVID-19与这些炎症反应联系起来,但我还没有看到令人信服的数据证明这一点。”
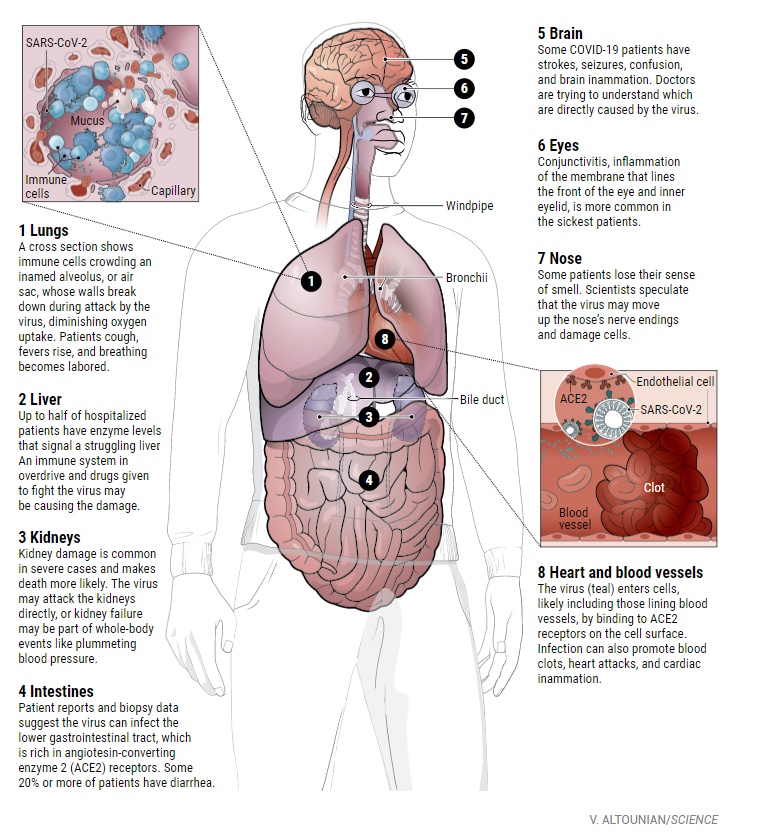
图片转自Science
他还担心抑制细胞因子反应的治疗方式可能会适得其反。目前美国已经开始进行针对特定细胞因子药物的临床试验。
但是Levitt担心这些药物可能会抑制人体对抗病毒所需的免疫反应。Levitt说:“一味的抑制正常的免疫反应产生的炎症因子就意味着允许病毒继续进行复制,这种治疗方式可能存在一定的风险。”
与此同时,一些科学家正在把注意力集中在一个完全不同的器官系统上——心脏和血管(心血管系统)。他们认为,这个系统才是导致一些病人病情迅速恶化的原因。
攻击心血管
在意大利布雷西亚(Brescia),一名53岁的妇女走进当地医院的急诊室,她出现了心脏病发作的所有典型症状,包括心电图出现明显的特征波,血液中的一种血液标志物也表明其心肌受损。
进一步的测试显示,她的心脏出现肿胀和瘢痕,左心室(通常是心脏的动力室)非常虚弱,只能泵出正常数量血液的三分之一。
当医生们在冠状动脉中进行染色,寻找可能导致心脏病发作的阻塞物时,他们没有发现任何异常。但是,另一项测试却揭示了其心脏受损的原因——这名女子患有COVID-19。
病毒到底是如何攻击心脏和血管的,至今仍是一个谜。但数十份的研究和论文证明这种损害在COVID-19患者中是很常见的。
3月25日发表在《JAMA Cardiology》(《美国医学会杂志心脏病学》)上的一篇论文记录了中国武汉416例住院的COVID-19患者中近20%的患者出现了心脏损伤,而另一篇在武汉的研究表明,36名ICU病人中有44%患者伴有心律失常。
这种破坏似乎延伸到了血液。根据4月10日发表在《Thrombosis Research》杂志上的一篇论文显示,在一家荷兰重症监护病房的184名COVID-19患者中,38%的患者血液凝结异常,近三分之一的患者已经有了血栓。
血凝块会破裂并落在肺部,阻塞重要的动脉,这种情况被称为肺栓塞,据报道已经有19名患者死于这种情况。
动脉血栓也会进入大脑,导致中风。哥伦比亚大学医学中心(Columbia University Medical Center)心血管医学研究员Behnood Bikdeli发现,许多病人体内D -二聚体(D -dimer)含量非常高,而D -二聚体是血凝块的副产品。

图片转自Pixabay
Bikdeli说:“随着我们的观察不断深入,我们发现血凝块是导致COVID-19患者病情严重程度和死亡率的主要因素。”
感染本身就可能导致血管收缩,有报告显示手指和脚趾缺血——血液流动减少,导致手指肿胀、疼痛和组织死亡。而在这种情况下,血栓的形成无疑会加重患者的病情。
在肺部,血管收缩可能有助于解释由COVID-19患者中出现的一种令人困惑的现象,即一些患者血液氧合素水平极低,但却没有喘不过气来的症状。
在疾病的某些阶段,这种病毒可能会改变帮助调节血压和收缩血管的激素平衡,所以氧气的吸收是被血管的收缩所阻碍,而不是被阻塞的肺泡所阻碍。
Levitt说:“有一种理论认为,病毒会影响血管生物学,这就是为什么我们会看到氧气水平非常低的原因。”
如果SARS-CoV-2针对的是血管,这也可以解释为什么那些先前就有血管损伤的患者,例如糖尿病和高血压患者,会面临更高的重症风险。
美国疾病控制与预防中心(CDC)最近对美国14个州住院病人的数据发现,住院病人中约有三分之一的人患有慢性肺病,几乎同样多的人患有糖尿病,近一半的人患有高血压。
宾夕法尼亚大学医院(HUP)肺部疾病专家Nilam Mangalmurti说:“令人震惊的是,ICU里没有大量哮喘患者或其他呼吸道疾病患者,疾病的风险因素似乎只与心血管相关疾病有关,包括糖尿病、肥胖、高年龄段、高血压。”
科学家们正在努力研究到底是什么导致了心血管损伤,并做出如下假设:
然而,实际上有关这方面的研究还在起步阶段,还有太多的问题无法解答,比如因为目前无法解释什么样的人更易受到损伤,为什么有些人感染后病症更重,为什么疫情在一些病人身上发展迅速,为什么有些患者的治疗非常难恢复等。
病毒的其他战场——肾脏
全球范围内对肺功能衰竭流行导致的呼吸机短缺的担忧引起了广泛关注。因此,为了尽可能保障患者的治疗,医院争相购买另一种设备:透析机。
纽约大学朗格尼医学中心的神经学家Jennifer Frontera说:“一般而言,COVID-19患者不是死于肺衰竭,他们就是死于肾衰竭。”肾脏由于富含ACE2受体,因此可能成为另一个病毒的靶器官。
目前,朗格尼医学中心已经治疗了数千名COVID-19患者,由于仪器的短缺,医院正在开发一种使用不同设备的透析方案,以支持更多患者的治疗。
据研究显示,武汉85名住院患者中有27%患有肾衰竭。另一份研究报告称,在中国湖北和四川两省近200名住院的COVID-19患者中,59%的患者尿液中含有蛋白质,44%的患者尿液中有血液,两者都表明了肾脏受损。
那些患有急性肾损伤(AKI)的患者,其死亡率是没有急性肾损伤的COVID-19患者的5倍多。
图片转自Pixabay
中国科学研究院苏州生物医学工程技术研究所神经科学家Hongbo Jia说:“尽管肺部是主要的‘战场’,但是一小部分病毒可能会攻击肾脏。就像在真正的战场上一样,部分病毒可能转移战场,如果两个部位同时受到攻击,每个部位都会受损很严重。”
在一项研究中,对患者的尸检发现,患者肾脏电子显微照片中存在病毒颗粒,这表明肾脏在感染过程中受到了直接攻击。
但肾脏损伤也可能是附带损害,呼吸机的治疗增加了肾脏损伤的风险;抗病毒药物包括正在COVID-19患者身上试验的remdesivir可能也同样会增加肾脏受损风险;细胞因子风暴也能显著减少流向肾脏的血液,造成致命的损伤。
而像糖尿病这样已经存在的疾病会增加肾脏受伤的几率。西北肾脏中心的首席医疗官Suzanne Watnick说:“对于已经患有慢性肾脏疾病的患者而言,他们转变为急性肾脏损伤的风险更高。”
病毒攻击大脑
COVID-19患者的另一组显著的症状集中在大脑和中枢神经系统。Frontera说,在所在的医院中有5%到10%的COVID-19患者需要神经科医生协助治疗。
但她认为这一数字可能远远低于神经受损的患者人数,因为其中许多患者服用了镇静剂和呼吸机,可能会掩盖神经上的不适症状。
Fronter见过COVID-19患者伴有脑炎、癫痫和“交感神经风暴”(交感神经系统的过度反应会导致癫痫样症状,通常见于脑外伤后的患者),还有一些COVID-19的患者会短暂地失去意识、中风、失去嗅觉等症状。
研究人员想知道,在某些情况下,感染是否会抑制脑干反射,对脑干反射的抑制也可以解释为什么有些病人在血氧水平极低的状态下,却并没有表现出气喘吁吁地呼吸空气的症状。
约翰斯·霍普金斯医学院(Johns Hopkins Medicine)的重症监护医师Robert Stevens说,ACE2受体同样存在于神经皮层和脑干中,但尚不清楚病毒是在什么情况下进入大脑并与这些受体相互作用的。
4月3日,一个来自日本的研究小组的案例研究在《International Journal of Infectious Diseases》上发表,研究人员在一名罹患脑膜炎和脑炎的19岁COVID-19患者的脑脊液中发现了新冠病毒,这表明该病毒也可以穿透中枢神经系统,造成脑部炎症。

图片转自Pixabay
但其他因素可能会损害大脑。例如,细胞因子风暴可能导致脑肿胀,血液凝块的剥离可能引发中风。
上个月,匹兹堡大学医学中心(University of Pittsburgh Medical Center)的神经病学家Sherry Chou组织了一个全球联盟,该联盟目前包括50个中心,从已经接受治疗的患者那里收集神经学数据。
早期目标很简单,确定住院病人中神经并发症的发生率,并记录他们的情况。Chou和她的同事希望收集扫描、实验室测试和其他数据,以更好地了解病毒对包括大脑在内的神经系统的影响。
Chou推测了一种病毒入侵大脑的可能途径,即通过鼻子,然后向上,通过嗅球,进入大脑(这也解释了部分患者出现嗅觉丧失的症状)。但同时Chou也认为,还需要更多的证据来证实这一路径发生的可能性。
病毒入侵肠道
3月初,一名71岁的密歇根州妇女从尼罗河旅游归来,她伴有腹泻、便血、呕吐和腹痛。起初,医生怀疑她有一种常见的胃肠疾病病,比如沙门氏菌感染。
但在她出现咳嗽症状后,医生通过鼻腔拭子检测发现其新型冠状病毒检测呈阳性。《The American Journal of Gastroenterology》( 《美国胃肠病学杂志》,AJG)在网上发表的一篇论文称,在胃镜检查中发现的粪便样本中病毒RNA呈阳性,同时也伴有结肠损伤的迹象,这表明新型冠状病毒会破坏胃肠道(Gl)。
实际上越来越多的证据表明,这种新型冠状病毒,可以感染下消化道的内壁,因为消化道细胞同样含有大量的ACE2受体。目前在多达53%的患者粪便样本中发现了病毒RNA。
《Gastroenterology》杂志上发表的一篇来自中国研究人员的论文报告显示,一名19岁的COVID-19患者的胃、十二指肠和直肠细胞组织活检中均发现了这种病毒的蛋白外壳。贝勒医学院的病毒学家Mary Estes认为,病毒能够在胃肠道中复制。
洛杉矶Cedars-Sinai医疗中心的Brennan Spiegel是AJG的联合主编,他说,最近的研究报告显示,多达一半的患者(各研究中平均约20%)出现腹泻症状。
Spiegel等人说,美国疾病控制与预防中心列出的COVID-19感染症状实际上并不包括胃肠道症状,这可能会导致一些COVID-19患者在初期只表现胃肠道疾病症状时被医生忽略了其可能已经感染SARS-CoV-2。

图片转自Pixabay
病毒在消化道的存在增加了其能够通过粪便传播的可能性。但目前还不清楚粪便中是否含有完整的传染性病毒,只能表明可以检出RNA和蛋白质。
爱荷华大学的冠状病毒专家Stanley Perlman说:“迄今为止,我们没有证据表明粪便传播的可能性。”
美国疾病控制与预防中心认为,根据非典型肺炎(SARS)和导致中东呼吸综合征(MERS)的病毒的经验,SARS-CoV-2在粪便传播的风险可能很低。
肠道并不是疾病在体内传播的终点。目前,超过三分之一的住院病人患上了结膜炎;其他报告显示患者伴有肝损伤;在中国两个中心住院的COVID-19患者中,超过一半的人体内的酶水平升高,表明肝或胆管损伤。
但是一些专家认为,这些多脏器损伤大多是由于病毒导致的身体机能衰竭时发生附属事件,如药物或免疫系统超负荷,就可能导致肝损伤。
这篇有关COVID-19对人体器官造成的破坏还仅仅是一个框架。还需要更多的研究,才能清晰地看到病毒真正的影响范围,以及它可能引发的心血管和免疫效应的连锁反应。随着科学的飞速发展,研究人员希望找到更全面的治疗方法。
参考资料:
“尽管现在每周都有1000多篇论文对SARS-CoV-2病毒及COVID-19进行探讨,但由于这种病毒的行为方式与人类所见过的任何病原体都不一样,所以很难对它有一个清晰的认识。”





-
病毒可能会直接攻击心脏和血管的内膜,因为心脏内膜和鼻子和肺泡一样富含ACE2受体; -
可能是由于肺部混乱造成的缺氧损害了血管结构; -
可能由于细胞因子风暴在破坏其他器官的同时也损伤了心脏。



https://www.sciencemag.org/news/2020/04/how-does-coronavirus-kill-clinicians-trace-ferocious-rampage-through-body-brain-toes#
https://covid19.who.int/
